 商务咨询:胡经理 18827669267
商务咨询:胡经理 18827669267
 版权所有:湖北长江瑞益医药科技有限公司
版权所有:湖北长江瑞益医药科技有限公司
 备案序号:鄂ICP备17026271号-2
备案序号:鄂ICP备17026271号-2
 公司地址:武汉东湖新技术开发区高新二路388号生物医药企业加速器C11栋1-6层
公司地址:武汉东湖新技术开发区高新二路388号生物医药企业加速器C11栋1-6层 2026 年 3 月,FDA 正式发布 《ANDA 外用药品理化与结构(Q3)表征研究》终版指南 ,将半固体制剂的 “微观结构” 纳入仿制药一致性核心评价体系,标志着外用仿制药审评从 “剂型对标” 迈入 “结构等效” 时代,对全球药企研发、申报与产业竞争格局产生深远影响。
一、政策核心:Q3 表征,破解外用制剂 “同剂型不同效” 难题
外用软膏、乳膏、凝胶等半固体制剂属于复杂仿制药,传统审评仅关注活性成分、剂型、给药途径一致,难以覆盖微观结构差异 —— 同样是 “乳膏”,可能是水包油 / 油包水不同乳剂结构;同样是 “软膏”,基质组成、流变行为、粒径分布千差万别,直接影响药物释放、皮肤渗透与临床疗效。
本次指南明确Q3 表征两大核心价值:
精准界定剂型:通过外观质地、相态、物质结构组织等基础表征,杜绝 “同名不同质” 的剂型混淆;
支撑生物等效性:覆盖流变行为、水活度、pH、晶型、转化相关性等 10 项全面指标,量化微观结构对药物性能的影响,直接关联 BE 论证。
指南将 Q3 对比结果分为相同性、相似性、差异三个层级,明确不同结果对应的 BE 证据要求:Q3 相同可大幅简化体内试验,Q3 相似需补充风险缓解证据,Q3 差异则难以通过审评,形成 “结构一致→疗效一致” 的科学审评链条。
二、产业影响:研发成本抬升,头部企业抢占技术高地
Q3 表征成为 ANDA 申报 “硬门槛”,直接重塑产业格局:
研发端:企业需配备显微成像、流变仪、粒径分析等专业设备,开展多批次对比研究,研发周期延长、成本增加,但减少体内临床试验,长期降低研发风险;
申报端:要求提交完整 Q3 对比数据至 eCTD 3.2.P.2 章节,资料准备更规范、严谨,倒逼企业提升质量研究能力;
竞争端:中小药企因技术、资金短板受限,具备完整 Q3 研究体系的头部企业将占据申报优势,行业集中度进一步提升。
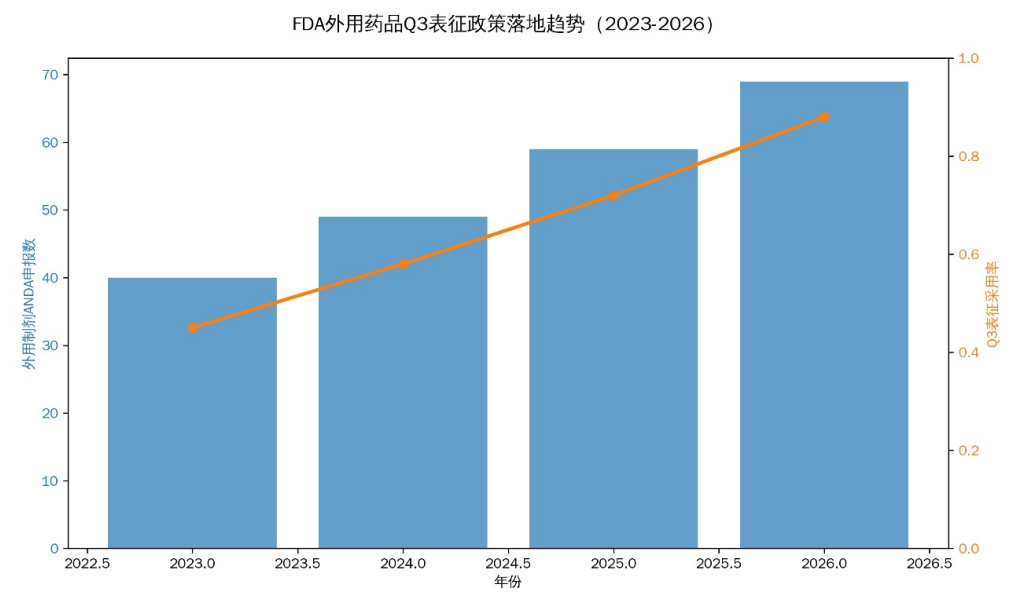
数据显示,2023-2026 年外用制剂 ANDA 申报量持续增长,Q3 表征采用率从 45% 飙升至 88%,政策落地效果显著。
三、中国药企启示:接轨国际标准,以技术创新破局
对于中国仿制药企业而言,Q3 指南既是挑战,更是出海合规的关键抓手:
提前布局 Q3 研究体系:针对痤疮、玫瑰痤疮等外用热门领域,同步开展维A酸类等药物的理化性质、结构表征,匹配 FDA 标准;
强化微观结构控制:优化处方与生产工艺,确保受试制剂与参比制剂 Q3 属性一致,降低 BE 失败风险;
主动沟通提升申报效率:通过受控函、ANDA 前会议与 FDA 对接,明确审评要求,缩短申报周期。
✨ 结 语
FDA Q3 指南的落地,是仿制药审评科学化、精细化的必然趋势,不仅解决外用制剂 “一致性评价” 核心痛点,更重新定义了全球仿制药研发的技术底线。中国药企唯有紧跟国际监管节奏,以微观结构创新突破技术壁垒,才能在国际仿制药市场中站稳脚跟,实现 “中国智造” 的高质量出海。
关注我们,持续解锁医药科技前沿,守护健康未来!