 商务咨询:胡经理 18827669267
商务咨询:胡经理 18827669267
 版权所有:湖北长江瑞益医药科技有限公司
版权所有:湖北长江瑞益医药科技有限公司
 备案序号:鄂ICP备17026271号-2
备案序号:鄂ICP备17026271号-2
 公司地址:武汉东湖新技术开发区高新二路388号生物医药企业加速器C11栋1-6层
公司地址:武汉东湖新技术开发区高新二路388号生物医药企业加速器C11栋1-6层 首次人体(first in human,FIH)试验,起始剂量的科学确定是保障受试者安全、风险控制的核心,同时也是试验药物科学、高效实施的关键关注点。
未观察到不良效应水平(No Observed Adverse Effect Level, NOAEL)作为动物毒理学研究中最核心的安全终点指标,其向人体起始剂量的换算方法,是目前全球药品监管机构(如 FDA、EMA、NMPA)和 ICH 指南(如 ICH S6 (R1)、ICH M3 (R2))推荐的经典路径。该方法通过系统消除种属间差异、放大安全边界,搭建起 “动物安全数据” 到 “人体首次给药剂量” 的可靠桥梁。

多国监管机构已经发布多项人体首次研究最大推荐起始剂量(maximum recommended starting dose, MRSD)指导文件。健康受试者中首次临床试验起始剂量的推算主要依据非临床安全性数据,通常以动物未见不良反应的剂量水平 (No Observed Adverse Effect Level,NOAEL)进行推算。
美国FDA 2005年指南Guidance for Industry Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers,详细介绍了健康人首次最大推介起始剂量的推算,通过标准化的算法,基于动物NOAEL推算人体HED,并应用安全系数得到MRSD。该过程旨在提供一致性和科学性,同时允许根据具体情况灵活调整。
一、NOAEL定义
严格定义:在规定毒理学试验条件下,通过对动物进行不同剂量组的暴露(急性、亚急性、亚慢性或慢性),未观察到与药物相关的、具有统计学意义或生物学意义的不良效应(毒性反应)的最高剂量水平。
数据来源于以下三类核心毒理学试验,且满足“数据可重复性、剂量梯度合理、观察指标全面”三大要求:
1.急性毒性试验(单次给药,观察 14 天):用于初步判断药物的毒性强度和靶器官,为长期毒性试验剂量设计提供参考;
2.亚慢性毒性试验(重复给药 28 天、90 天等):核心数据源,可全面评估药物重复暴露后的毒性特征、靶器官损伤及可逆性,NOAEL 多来源于此;
3.慢性毒性试验(重复给药 6 个月以上,多用于肿瘤药、慢性病治疗药):针对长期给药的药物,提供更贴近临床用药场景的 NOAEL 数据。
二、换算原理:种属差异校正
动物与人体在体型、药物代谢酶活性(如 CYP450 家族)、受体密度、组织分布特征等方面存在显著差异,直接将动物 NOAEL 作为人体起始剂量会带来巨大安全风险(如小鼠对某些药物的耐受性是人体的数十倍)。因此,换算的核心逻辑是 “两步法” :先通过 “种属换算系数” 消除动物与人体的生理差异,再通过 “安全系数” 抵御未知的种属间毒性反应差异及人体个体差异。
1.种属换算系数的选择:体表面积法
目前全球指南(ICH S6 (R1))明确推荐体表面积法作为 NOAEL 种属间换算的首选方法,其核心优势是:药物的毒性反应(尤其是与代谢相关的毒性)与机体体表面积的相关性远高于体重 —— 体表面积能更科学地反映药物在体内的分布、代谢速率及暴露总量。体重法仅在缺乏体表面积数据时作为替代(如部分大型动物),但误差较大。
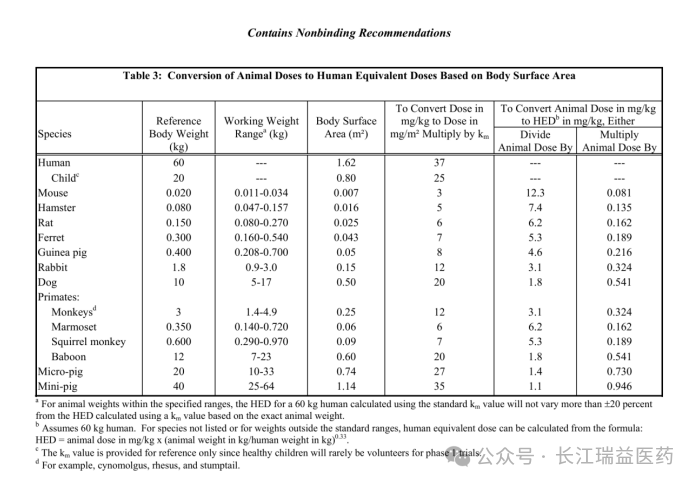
常用实验动物与人体的体表面积换算系数(来源ICH S6 (R1) 附录)如下:
小鼠对应的动物→人体体表面积换算系数为 0.08,常用于小分子药急性毒性试验;大鼠为 0.16,是亚慢性毒性试验首选动物的换算系数;犬为 0.54,适用于生物药、小分子药长期毒性试验;猴(食蟹猴 / 恒河猴)为 0.32,是生物药(如单抗)核心毒性试验动物的换算系数。
2.安全系数的科学设定
安全系数是 FIH 试验起始剂量 “保守性” 的核心保障,其设定需综合评估药物类型、毒性特征、非临床数据充分性、种属间毒性反应一致性及临床风险等因素,而非固定值。
ICH M3 (R2) 指南给出了安全系数的参考范围及调整逻辑:
低风险药物对应的安全系数参考范围为 10~20 倍,适用于小分子仿制药、me-too 药,这类药物非临床数据充分(涵盖急性 + 亚慢性毒性),种属间毒性反应一致;
中风险药物的安全系数参考范围为 30~50 倍,适用于新机制小分子药、生物类似药,非临床数据较充分,毒性靶器官为非关键器官(如皮肤、胃肠道);
高风险药物的安全系数参考范围为 50~100 倍,适用于 First-in-class 药物、生物药(单抗、双抗、ADC)、细胞治疗药,这类药物非临床数据有限,毒性靶器官为关键器官(肝、肾、心脏、中枢神经)。
特殊调整场景:若动物毒性反应为人体罕见反应(如大鼠特有的晶状体毒性),安全系数可适当降低(如从30倍降至 20 倍);若药物存在活性代谢产物(且代谢产物毒性高于母药),安全系数需提高(如从30 倍升至 50 倍);若非临床数据显示毒性反应具有剂量依赖性且可逆性差,安全系数需放大至 80~100 倍。
三、案例
案例1:小分子靶向药
某EGFR抑制剂,大鼠90天亚慢性毒性试验 NOAEL=40mg/kg,计划采用体表面积法换算人体起始剂量:
1.确定换算系数:大鼠→人体体表面积换算系数为 0.16;
2.设定安全系数:新机制小分子药,毒性靶器官为皮肤(痤疮样皮疹),风险等级为中,安全系数取 30;
3.计算:40mg/kg × 0.16 ÷ 30 ≈ 0.213mg/kg;
4.剂量圆整:临床给药剂量需便于操作,圆整为 0.2mg/kg(或按体表面积换算为12mg/m²,成人 70kg 体表面积约 1.8m²,即21.6mg /人,圆整为 20mg / 人)
案例2:PD-1单抗
某抗PD-1单抗,食蟹猴13周重复给药毒性试验 NOAEL=10mg/kg,换算过程:
1.换算系数:猴→人体体表面积换算系数为0.32;
2.安全系数:First-in-class 生物药,毒性靶器官为免疫系统(免疫相关不良反应),风险等级为高,安全系数取60;
3.计算:10mg/kg× 0.32 ÷ 60 ≈ 0.053mg/kg;
4.剂量圆整:考虑生物药给药剂量精准性,设定为 0.05mg/kg(或 3.5mg/70kg成人,圆整为 5mg/人)。
四、换算过程关键注意事项
(一)关键注意事项
1.动物种属选择的合理性:优先选择相关/敏感种属,与人体药物代谢、毒性反应更接近的种属。单一物种数据换算的不确定性高于多物种数据整合。
2.毒性反应的生物学关联性:需评估动物 NOAEL 对应的 “无毒性反应” 是否与人体潜在毒性具有生物学关联 —— 若动物反应为种属特异性(如小鼠的颌下腺毒性),需结合其他物种数据调整换算逻辑。
3.与其他方法的交叉验证:对于高风险药物,建议将NOAEL换算结果与 MABEL、药理学活性剂量(PAD)换算结果交叉验证,取最小值作为起始剂量。
(二)常见误区
1.安全系数 “一刀切”:无论药物风险高低均采用30倍安全系数,忽略了 First-in-class药物与仿制药的风险差异;
2. 忽略毒性反应的可逆性:对于可逆性毒性(如短期胃肠道反应),安全系数可适当降低;对于不可逆毒性(如肝纤维化),需大幅提高安全系数,避免因评估不足导致风险。
五、总结
ICH S6 (R1)(生物药非临床安全性评价)明确指出:“对于生物药,NOAEL 换算时应优先采用与人体靶点亲和力、受体密度更接近的种属(如猴),安全系数可根据种属间交叉反应性调整”;ICH M3 (R2)(支持药物临床试验的非临床安全性研究)强调:“FIH 起始剂量的确定需综合 NOAEL、药理学活性数据、药代动力学特征,安全系数的设定应体现风险分级原则”。
基于NOAEL的换算,是FIH试验起始剂量计算的 “基础盘”—— 其核心是通过体表面积法校正种属差异,通过风险分级设定安全系数,实现“安全优先、科学保守” 的目标。对于低风险药物,该方法可直接作为起始剂量确定的核心依据;对于高风险药物(如生物药、First-in-class 药物),需与 MABEL、药理学活性剂量等方法结合,形成多维度验证,确保起始剂量既规避安全风险,又能为后续剂量递增提供有价值的暴露量数据。
关注我们,持续解锁医药科技前沿,守护健康未来!